Модификация аптамеров
Существует два альтернативных пути модификации аптамеров - до отбора [3, 67, 68] и после него [3, 69]. При введении модификаций до первого раунда SELEX важно, чтобы полученная модифицированная комбинаторная библиотека была устойчива в условиях проведения отбора и участвовала в реакциях стадии амплификации. Модификации, которые вводят в последовательность полученного аптамера, не должны снижать его аффинность и специфичность к молекуле-мишени.
Для введения модифицированных нуклеотидов в последовательность комбинаторной библиотеки или полученного аптамера используют мутантные аналоги ДНК- или РНК-полимераз, эффективно включающие модифицированные нуклеозидтрифосфаты в олигонуклеотидную цепь, или подбирают условия, в которых природные полимеразы будут эффективно включать модифицированные нуклеозидтрифосфаты.
На данный момент существуют различные типы модификаций как комбинаторных библиотек, так и индивидуальных аптамеров, удовлетворяющие вышеперечисленным условиям.
Для придания аптамерам новых свойств наиболее часто используют введение заместителей по С5-положению пиримидиновых нуклеотидов исходной библиотеки [66, 70] (рис. 3).
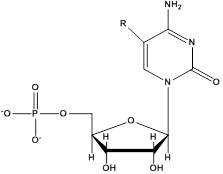
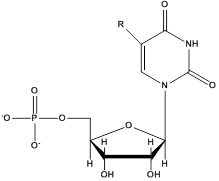
С5-модифицированный цитидин С5-модифицированный уридин
Рис. 3. С5-Модифицированные пиримидиновые нуклеотиды.
Такие модификации позволяют получить аптамеры к молекулам-мишеням, для которых отбор аптамеров с использованием немодифицированной олигонуклеотидной библиотеки невозможен. Так, несмотря на то, что олигонуклеотиды являются полианионами, введение в состав исходной библиотеки олигонуклеотидов в С-5 положение положительно заряженного заместителя позволяет получить аптамер к отрицательно заряженным молекулам-мишеням [71]. Возможно также получение аптамеров, ковалентно связывающихся с молекулой-мишенью. Для этого используют библиотеки олигонуклеотидов, которые содержат фотоактивируемые группы, например, бром или йод [72]. С-5-Модифицированные пиримидиновые нуклеозидтрифосфаты узнаются как природными, так и мутантными полимеразами, что позволяет использовать их в процессе отбора [73]. При сравнении сродства модифицированного и не модифицированного аптамеров к одной и той же молекуле-мишени Kd комплексов белков с С5-модифицированными аптамерами может отличаться от Kd комплексов тех же белков с немодифицированными аптамерами как в большую, так и в меньшую сторону [66].
Для повышения устойчивости аптамеров к эндонуклеазной деградации широко используют введение модификаций по 2'-положению, таких как 2'-OCH3, 2'-NH2 или 2'-F (рис. 4) [3, 66]. Модифицировать по 2'-положению можно как исходную, так и обогащенную библиотеку олигонуклеотидов.
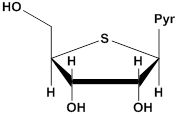
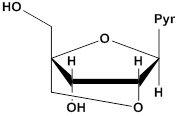
'-тионуклеозид LNA
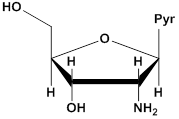
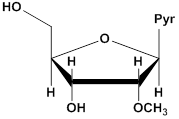
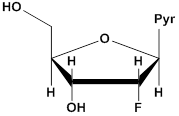
'-аминонуклеозид 2'-О-метилнуклеозид 2'-фторнуклеозид
Рис. 4. Модификации рибозного остатка пиримидиновых (Pyr) нуклеозидов.
Аптамеры, содержащие 2'-NH2-модифицированные пиримидиновые нуклеотиды, более стабильны в сыворотке крови по сравнению с немодифицированными РНК-аналогами [74], однако такая модификация снижает термодинамическую стабильность дуплексной части как ДНК-, так и РНК-аптамеров [75]. 2'-OCH3-Модифицированные нуклеотиды широко используются для повышения нуклеолитической стабильности как индивидуальных аптамеров [67], так и исходных олигонуклеотидных библиотек [76]. Их синтез дешевле, чем синтез 2'-NH2- и 2'-F-содержащих нуклеотидов, а 2'-OCH3-модифицированные аптамеры обладают высокой аффинностью и стабильностью в биологических средах. Более того, 2'-O-метилированные рибонуклеотиды встречаются в природе в рибосомальных и транспортных РНК млекопитающих [77]. Другой модификацией, повышающей стабильность РНК-аптамеров в биологических средах, является замена 2'-OH группы на 2'-F [49, 67]. 2'-F-Модифицированные пиримидиновые нуклеотиды были использованы для получения Macugen - первого аптамера, прошедшего клиническую проверку [67], и anti-Factor IXa аптамера [78], который сейчас проходит клинические испытания. 2'-F-Модифицированные олигорибонуклеотиды не токсичны in vivo [77]. LNA-содержащие олигонуклеотиды также можно отнести к 2'-модифицированным НК [79]. Они способны участвовать в реакции транскрипции и ПЦР, их дуплексы отличаются высокой термостабильностью [79]. Введение LNA-нуклеотидов существенно повышает стабильность модифицированных олигонуклеотидов в биологических средах. Исследование токсичности LNA-содержащих олигонуклеотидов пока не завершено [77]. Вышеупомянутые 2'-модифицированные нуклеотиды могут быть включены в состав аптамеров как химическим [66, 80], так и химико-ферментативным путем с использованием мутантных полимераз [66, 76] или природных полимераз в соответствующих условиях [1, 66, 67, 74].